

活體熒光多重成像分析可以對小動物活體狀態下的生物過程進行組織⛵️😂、細胞和分子水平的定性和定量研究,是輔助科研人員理解疾病發生機製、進行藥物研發和臨床精確診斷的重要技術。然而在實際應用中🪯,該技術仍面臨著成像深度淺👎、分辨率差👷、對比度低和可檢測通道數量少等諸多挑戰♿️,其中缺乏光譜分離的近紅外熒光探針是製約這一技術進步的重要因素⏭。那麽🧘♀️,能否開發出一套光譜分離的近紅外熒光探針工具🩼,讓科學家們可以更全面地窺視活體動物中的生命活動呢🧍♂️?
2021年7月29日🚴🏼♀️,沐鸣开户張凡教授團隊(沐鸣开户博士生王婷👸🏻、博士後王尚風為第一作者)在Nature Materials雜誌上發表文章 A hybrid erbium (III)-bacteriochlorin near-infrared probe for multiplexed biomedical imaging(鉺-細菌葉綠素雜化近紅外熒光探針用於生物醫學多重成像),為以上難題的攻克提供了全新的思路與可能🀄️。

技術進步:近紅外熒光成像逐步應用於活體多重檢測分析
熒光是自然界中的一種光致發光現象。因其靈敏度高💱,分辨率好且具有實時性等特點👩🦼➡️,熒光成像在生命科學、藥學和醫學診斷等領域都有著非常廣闊的應用前景。借助於多種熒光探針的標記📓,人們還能同時通過多個不同波長的信號組合,實現多個待測物的同時多通道檢測🎋🏄♂️。
過去,體外診斷或者細胞成像是研究者們的主要目的,因而傳統的可見光(波長400~700 nm)區熒光探針即可滿足要求🛡。隨著科學研究的不斷深入🏃🏻♂️,人們越來越需要理解活體動物原位微環境的生物學機製,但由於生物體內不同的組織(如皮膚、脂肪、骨骼等)對激發光和發射光均具有不同程度的散射和吸收作用🧏🏿🚵🏿♀️,使得在這個區間內的光學穿透深度和成像分辨率都不理想🎯。這種現象就好比是在大霧天看風景🧑🏽🎨,不僅看不清也看不遠👩🦳。
近些年來☣️🖐🏿,近紅外(波長700~1700 nm)窗口逐漸被證實是一個生物組織的光學“透明”窗口。近紅外光在穿透皮膚、脂肪和骨骼等生物組織時發生的散射和吸收現象均較少🎈,因而相對於可見光而言其“折損率”更低。不僅如此👨🏽🏫,在近紅外區域,來自於生物體內各種色素的自發熒光也極大的降低。在這兩大優勢的助力下🎉,近紅外區域內的熒光成像在活體動物研究中有著較好的表現與巨大的發展前景。
然而在實際應用中👨🏽✈️🤷🏿♀️,近紅外活體熒光多重成像仍舊不理想,其潛力還未得到完全釋放。當前使用的熒光探針普遍光譜較寬🏃🏻,吸收發射挨的近,因而無法對生物組織進行無串擾的多重標記與成像🚶🏻♂️➡️。
研究突破🤷🏽♂️🧑🔧:構建光譜分離的近紅外熒光探針實現高對比度的活體多重成像
針對以上難題,張凡團隊開發了一種基於稀土鉺離子與細菌葉綠素配位的新型近紅外熒光探針體系🌎,實現了光譜分離的活體熒光多重成像🤵🏿👨🏿🦳。稀土鉺離子配合物具有1530納米左右的近紅外二區特征單色發光特性,理論上非常適合用來進行活體熒光成像研究。然而要在生理環境下實現這一發光卻並不容易。傳統的分子構建策略不僅容易導致鉺離子的發光被水分子淬滅,而且分子的激發波長常常在紫外光區,無法在活體成像中進行應用。研究人員發現自然界中的紫細菌能夠利用細菌葉綠素高效地捕捉近紅外光並將光能轉換為化學能。受此啟發🥷🏿,張凡團隊提出了以細菌葉綠素作為天線配體敏化稀土鉺離子的新穎策略,所構造出的熒光探針不僅能在水相中發射出明亮的近紅外熒光,而且其吸收和發射半峰寬小於32納米🧜🏼,斯托克斯位移值達到了760納米🍷,為活體熒光多重成像的實現提供了強有力的研究工具🍁。
團隊利用超快光譜技術和低溫磷光光譜分析揭示了細菌葉綠素和鉺離子之間存在高效的三重態能量轉移過程,並且進一步通過分子工程調控了配體的吸收,驗證了圍繞鉺-細菌葉綠素體系開發多色可調近紅外熒光探針工具的可行性💅🏿。
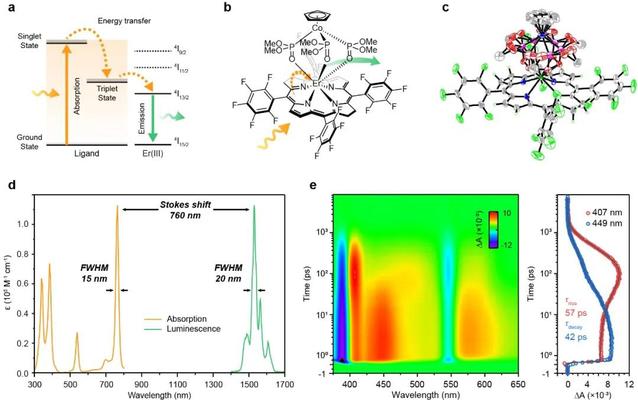
圖1:(a)鉺-細菌葉綠素配合物的能量傳遞機理圖;(b)鉺-細菌葉綠素配合物的代表性分子EB766的化學結構式🍍;(c)EB766的單晶結構;(d)EB766的吸收和發射光譜圖🦍;(e)超快瞬態吸收光譜表征EB766的激發態動力學過程。
最後🕵🏿♂️,團隊基於探針優異的光學特性和生物相容性進行了生物成像研究🧜🏽。探針較窄的吸收光譜特性使得通過正交激發控製的多重成像方法可以清晰地勾勒出小鼠血管和淋巴管的精細結構及其空間位置關系,並能實時顯現胃腸道消化系統和血液循環系統的代謝活動。該方法有望為手術導航和臨床診斷提供更精準的信息🈶。團隊進一步利用新型探針標記了小鼠體內的癌細胞,探針較窄的發射光譜特性也讓正交發射控製的多重成像方法得以在小鼠腦部以無創傷的方式清晰地觀察到癌細胞的運動、遷移、以及在血管壁上駐紮等過程。相比於原先的研究方法,這種方法有效地避免了開視窗造成的組織損傷,以及昂貴的成像設施,為活體水平的細胞互作研究提供了新的研究平臺。
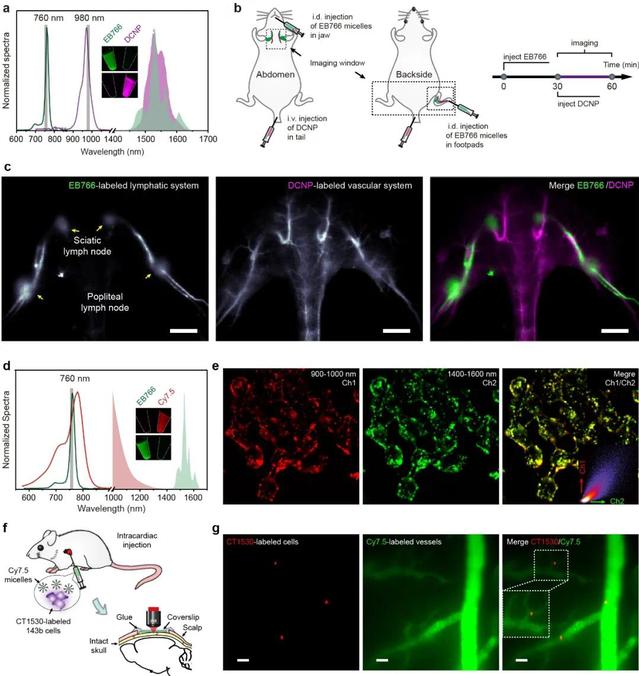
圖2:(a-c)基於新型近紅外熒光探針構建的激發光譜分離多重成像方案,實現了小鼠血管和淋巴管結構的高分辨率成像☞;(d-g)基於新型近紅外熒光探針構建的發射光譜分離多重成像方案🤘🏽🧎🏻➡️,實現了癌細胞在小鼠腦部轉移的動態實時可視化觀察。
目前🗞,盡管該研究已經取得了較好的初步應用效果👨👩👧,未來還需要更進一步地提高探針的發光效率🛝,增加顏色通道以更好的滿足活體內高通量多重檢測的應用需求。此外👨🏿🦲,改善探針分子的功能修飾特性,增強與前沿生物與成像技術的兼容性等問題仍然有待後續研究。但是這一科研成果所點亮的諸多可能,都將為化學與材料科學、生物醫學光子學、生命科學、生物醫學工程和醫療診斷等領域拓寬研究視野與前行的方向。
原文鏈接:
https://www.nature.com/articles/s41563-021-01063-7





